-


化学小分子CDMO服务
化学小分子CDMO:现代药物研发的基石
-
小分子药物凭借优异的生物利用度、成熟的生产工艺以及明晰的监管路径,在医药行业持续占据主导地位。在此背景下,小分子CDMO作为关键角色在加速创新、应对工艺复杂性以及推动规模化生产方面发挥着至关重要的作用。
作为值得信赖的小分子CDMO合作伙伴,我们为制药和生物技术客户提供覆盖药物研发全生命周期的支持服务——从早期药物发现、工艺开发到商业化生产。 我们始终秉持创新驱动与合规为本的理念,提供高质量的起始原料(RSM)、中间体、原料药(API)、高活性API(HPAPI)及制剂一站式解决方案。 我们的一体化平台助力小分子从实验室加速走向市场。

一站式小分子CDMO平台
从发现到商业化,我们全面整合小分子CRO与CDMO能力,提供涵盖起始原料、中间体、API、高活性API及制剂在内的全流程(端对端)服务。
绿色化学与前沿技术
精通手性分子、高活性API、杂环和ADC连接子等复杂分子的合成,辅以流动化学、高通量筛选、生物催化、制剂增溶技术等前沿技术平台。
全球合规与成本效益
我们拥有符合GMP标准的生产基地,确保在监管合规方面达到卓越水平。我们为客户量身定制CDMO策略,有效降低成本、减少技术转移环节,加快产品上市进程。
我们的服务
我们依托深厚的化学专业积累与全球合规经验,深耕小分子CDMO领域,帮助客户加速项目进程,控制风险,把握市场先机。
我们的服务项目包括
早期研发服务
- 精通复杂合成路线
- 提供Full-Time Equivalent(FTE)和Fee for Service(FFS)服务
- 高性价比与高效交付
- IP保护
工艺开发
- 工艺路线筛选与优化
- 工艺可放大性强,兼顾经济性
- 无缝衔接至GMP生产阶段
- 技术转移与放大全流程支持
原料药与中间体生产
- 产品涵盖抗肿瘤、抗病毒、糖尿病、胃肠道和心脑血管疾病治疗等领域
- 符合GMP标准的设施
- 出色的合成能力
高活性API生产
- 符合OEB-5标准的HPAPI车间
- 丰富的高活性化合物操作经验
制剂生产
- 口服固体制剂:片剂、硬胶囊、颗粒、粉末;半固体制剂:乳膏、软膏和凝胶
- cGMP生产
- 增溶技术(热熔挤出、喷雾干燥)
- 20年的丰富经验
- 服务超过200个新药制剂项目
注册CMC支持
- 支持IND/NDA申报资料撰写
- 支持中美双报等多区域注册
- 符合eCTD格式的申报文档支持
- 协助客户与监管机构沟通交流
分析开发与质量控制
- 方法开发与验证全面覆盖
- 稳定性研究与ICH指导原则检测服务
- 起始原料、中间体、原料药及制剂放行检测
- 配备齐全分析仪器
我们的基地
研发基地





生产基地
•口服固体:4个车间,年产能约10亿单位
•半固体外用制剂:3个车间,年产能约5,000万支
•固体分散体生产线:1个
•服务剂型:片剂、硬胶囊、颗粒、散剂、乳膏剂、软膏剂和凝胶剂及靶向抗肿瘤制剂专线
•支持批量从~3,000片(粒)至约300万片(粒)
医药中间体 Non-GMP 生产
•反应釜数量:~50台,反应釜规格 500L - 5,000L
•反应釜总体积:~115,000L
•反应类型: 格氏反应、氧化反应、氯化反应、加氢反应、高压氢化反应、超低温
反应和重氮化反应等
Site1: 安徽马鞍山研发中心
高活原料药、ADC Payload-Linker类GMP生产
•5条GMP高活生产线,玻璃反应釜总体积>4,000L;2条GMP非高活公斤级生产线;共6个D级洁净区
•生产规模涵盖公斤级早期至商业化规模
•高活车间都配备符合国际OEL管理规范的负压隔离器,可满足生产OEB5, OEL 0.01μg/m3化合物的防护要求
•满足FDA/EMA/NMPA质量体系标准,已通过1次欧盟QP审计
Site2: 安徽马鞍山产业化基地
关键起始物料、中间体、原料药、多肽类GMP生产
•反应釜数量:~170台,反应釜规格100L-8,000L
•反应釜总体积: ~483,000L ,拥有D级洁净区
•反应类型:氢化、格氏、氧化,以及高温(240°C)、深冷(-80°C)、光照反应等
案例研究
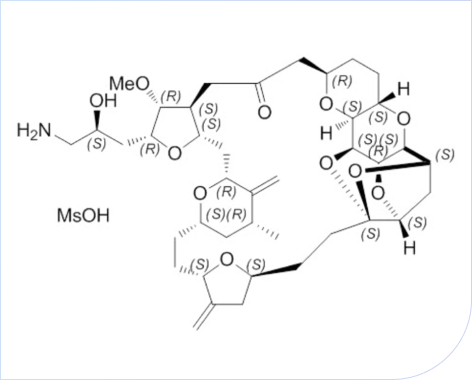
艾立布林全合成技术突破:19个手性中心结合,62步合成工艺
• 完成了原料药及高级中间体的工艺开发、中试生产、百克级的 GMP 工艺验证和稳定性试验
• 工艺所取得的 API 与原研相比,特征杂质限度均在 0.10% 以下
• 可提供 GMP 体系及 non-GMP 体系下,艾立布林高级中间体及 API 的百克级稳定供应
• 已获得2个相关FDA DMF备案(MF033836, MF037054), 该项目欧洲ASMF和美国USDMF已经批准上市
常见问题解答
原料药(API)是药物中具有药理活性的化学物质,是药物发挥治疗作用的核心成分。制剂则是将原料药与辅料(如淀粉、乳糖等)按一定比例混合,制成便于患者使用的最终药物形式,如片剂、胶囊、注射液等。简单来说,原料药是"药效成分",制剂是"成品药物"。
我们在复杂小分子化学合成领域具备深厚专业实力,专门处理手性分子、高活性化合物(HPAPIs)、杂环化合物、ADC载荷等具有挑战性的化学结构。我们的技术平台包括连续流化学、高通量筛选 (HTE)、生物催化、制剂增溶技术等前沿工艺。同时配备完善的分析检测能力,确保从起始原料到最终产品的全程质量控制。
我们建立了完善的cGMP质量管理体系,生产设施符合FDA、EMA、NMPA等国际监管标准。严格执行ICH指导原则,建立了完整的质量风险管理和偏差处理流程。我们具备专业的稳定性研究能力,为客户提供从IND到NDA的全程合规支持,协助客户在全球主要市场顺利获得监管批准。